Strukturaufklärung von Biomolekülen in ihrer natürlichen Umgebung
Wissenschaftler des Helmholtz Zentrums München und der Technischen Universität München (TUM) unter Leitung von Prof. Michael Sattler haben ein neues Verfahren entwickelt, mit dem die räumliche Struktur von Eiweißmolekülen in Lösung effizient bestimmt werden kann. Die Methode ist flexibel und generell anwendbar, um Strukturinformationen für Eiweiße und deren Bindungspartner in Signalwegen und in der Regulation der Genexpression zu gewinnen. Die Ergebnisse sind in der Fachzeitschrift Angewandte Chemie publiziert.
Die meisten größeren Eiweiße (Proteine) besitzen eine komplexe räumliche Struktur, bei der verschiedene kompaktere Untereinheiten durch flexible Ketten miteinander verbunden sind. Diese Flexibilität ist wichtig, um die Wechselwirkung von Eiweißmolekülen untereinander oder mit Reaktionspartnern zu regulieren. Bei der klassischen Strukturbestimmung durch Röntgenstrukturanalyse sind die Eiweißmoleküle in ein starres Kristallgitter eingebaut, was die Flexibilität der Untereinheiten verhindert oder zumindest beeinflusst. Um die Funktion der Eiweißmoleküle in ihrer natürlichen Umgebung zu verstehen, müssen daher Verfahren herangezogen werden, die die Struktur dieser Moleküle in Lösung untersuchen.
Das Team um Prof. Dr. Michael Sattler, Direktor des Instituts für Strukturbiologie am Helmholtz Zentrum München und Leiter des Bayerischen NMR-Zentrums an der TU München, kombinierte nun mehrere bekannte Verfahren zu einer effizienten Strategie für die Bestimmung der räumlichen Struktur von Biomolekülen in Lösung. Grundlage des Verfahrens ist die biomolekulare NMR-Spektroskopie (Magnetische Kernspinresonanz). "Die NMR-Spektroskopie ist die einzige Methode, die es erlaubt, atomare Details der Raumstruktur von Biomakromolekülen in Lösungen zu bestimmen", erklärt Prof. Sattler.
Analysiert man Proteine oder Proteinkomplexe mit einem NMR-Spektrometer, so erhält man aufgrund ihrer Größe zunächst eine Vielzahl sich gegenseitig überlagernder, kaum auswertbarer Signale. Mit einer vierstufigen Strategie, die die Wissenschaftler in ein gängiges Softwareprogramm zur Auswertung von NMR-Messungen integrierten, können Michael Sattler und sein Team die Signale nun trennen und so eine realitätsnahe Struktur ableiten.
Im ersten Schritt des neuen Verfahrens sammeln die Wissenschaftler existierende Strukturinformationen für die Untereinheiten. Diese stammen beispielsweise aus Röntgenstrukturanalysen oder konventionellen, NMR-basierten Strukturbestimmungen. In den nächsten Schritten wird bestimmt, wie diese Untereinheiten räumlich zueinander angeordnet sind. Hierzu werden zwei verschiedene Arten von Informationen ausgenutzt, die durch NMR-Experimente bestimmt werden können. So genannte Dipolare Restkopplungen geben Informationen über die relative Orientierung der einzelnen Untereinheiten des Komplexes.
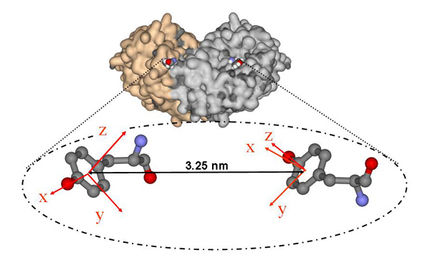
An mehreren Stellen des Proteins führen die Wissenschaftler im nächsten Schritt Nitroxyl-Gruppen ein, Moleküle, die ein ungepaartes Elektron besitzen. Diese lösen so genannte Paramagnetische Relaxationsverstärkungen aus und erlauben es, auch größere Abstände zwischen den Untereinheiten zu messen und dadurch die dreidimensionale Struktur des Proteinkomplexes aufzuklären.
Dieses Verfahren wandte das Team auf zwei strukturelle Module des menschlichen Spleißfaktors U2AF65 an. Spleißfaktoren sind bei der Regulation der Genexpression entscheidend und tragen unter anderem dazu bei, dass aus einem Gen unterschiedliche Proteine gebildet werden können. Aus der geschickten Kombination der NMR-Daten konnte die Struktur des Komplexes berechnet werden. Dabei zeigte sich, dass die Struktur in Lösung deutlich von der durch Röntgenstrukturanalyse bestimmten Struktur abweicht. "Unsere Methode ist generell auf viele Proteinkomplexe anwendbar, auch wenn sie sehr groß sind oder aus mehreren Untereinheiten bestehen", sagt Sattler. "Wir können dadurch biologische Regulationsmechanismen untersuchen, bei denen schwache und kurzlebige Wechselwirkungen eine wichtige Rolle spielen." Proteine sind keine starren Strukturen, sondern beweglich, damit sie Reaktionspartner binden und wieder freisetzen können. Diese dynamischen Effekte spielen eine wichtige Rolle für die molekulare Erkennung vieler biologischer Prozesse.
Daher ist das Verfahren für die Forschung von großem Nutzen: Die Charakterisierung der Struktur und Wechselwirkungen von Proteinen mit Bindungspartnern gibt Aufschluss darüber, wie Stoffwechselprozesse ablaufen und Krankheiten entstehen und liefern damit eine Grundlage für die Entwicklung neuer Medikamente.
Die Arbeiten wurden unterstützt aus Mitteln der EU (3D Repertoire, Functional and Structural Genomics of Viral RNA) und der Deutschen Forschungsgemeinschaft (DFG). Prof. Michael Sattler ist Mitglied des Exzellenzclusters Center for Integrated Protein Science Munich (CIPSM).
Originalveröffentlichung: Simon B, Madl T, Mackereth CD, Nilges M and Sattler M.; "An efficient protocol for NMR-based structure determination of protein complexes in solution"; Angew. Chem. Int. Ed. Engl. 2010.
Diese Produkte könnten Sie interessieren
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Aufschluss
Der Aufschluss von Proben ist ein kritischer Schritt in der chemischen Analytik, der oft über den Erfolg oder Misserfolg einer Untersuchung entscheidet. Es handelt sich dabei um die gezielte Umwandlung und Vorbereitung einer Probe, um die interessierenden Komponenten für die Analyse zugänglich zu machen. Durch verschiedene Verfahren wie die thermische, chemische oder enzymatische Aufschlussmethode werden Matrixkomponenten aufgelöst, unerwünschte Bestandteile entfernt und Zielsubstanzen freigesetzt.

Themenwelt Aufschluss
Der Aufschluss von Proben ist ein kritischer Schritt in der chemischen Analytik, der oft über den Erfolg oder Misserfolg einer Untersuchung entscheidet. Es handelt sich dabei um die gezielte Umwandlung und Vorbereitung einer Probe, um die interessierenden Komponenten für die Analyse zugänglich zu machen. Durch verschiedene Verfahren wie die thermische, chemische oder enzymatische Aufschlussmethode werden Matrixkomponenten aufgelöst, unerwünschte Bestandteile entfernt und Zielsubstanzen freigesetzt.