Neuer Sensor erkennt seltene Metalle in Smartphones
Eine effizientere und kostengünstigere Methode zum Nachweis von Lanthaniden, den in Smartphones und anderen Technologien verwendeten Seltenerdmetallen, könnte mit einem neuen proteinbasierten Sensor möglich sein, der seine Fluoreszenz verändert, wenn er an diese Metalle bindet. Ein Forscherteam der Penn State entwickelte den Sensor aus einem kürzlich beschriebenen Protein und nutzte ihn anschließend, um die Biologie von Bakterien zu erforschen, die Lanthanide verwenden. Eine Studie, die den Sensor beschreibt, erscheint in Journal of the American Chemical Society.
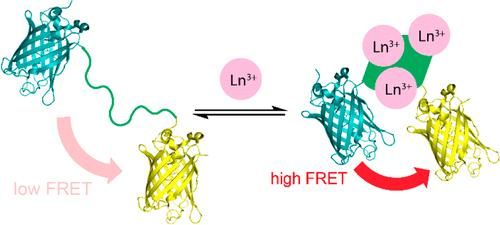
Ein neuer Sensor ändert seine Fluoreszenz, wenn er an Lanthanide (Ln), Seltenerdmetalle, die in Smartphones und anderen Technologien verwendet werden, bindet, was möglicherweise eine effizientere und kostengünstigere Methode zur Erkennung dieser schwer fassbaren Metalle bietet.
Cotruvo Lab, Penn State
"Lanthanide werden in einer Vielzahl von aktuellen Technologien verwendet, einschließlich der Bildschirme und der Elektronik von Smartphones, Batterien von Elektroautos, Satelliten und Lasern", sagte Joseph Cotruvo, Jr., Assistant Professor und Louis Martarano Career Development Professor für Chemie am Penn State und Senior Author der Studie. "Diese Elemente werden als seltene Erden bezeichnet, und sie beinhalten chemische Elemente mit einem Atomgewicht von 57 bis 71 im Periodensystem. Seltene Erden sind schwierig und teuer in der Gewinnung aus der Umwelt oder aus industriellen Proben, wie z.B. Abwässern aus Bergwerken oder Kohleabfällen. Wir haben einen proteinbasierten Sensor entwickelt, der winzige Mengen an Lanthaniden in einer Probe erkennen kann und uns wissen lässt, ob es sich lohnt, Ressourcen zu investieren, um diese wichtigen Metalle zu gewinnen."
Das Forschungsteam hat einen Fluoreszenzsensor zum Nachweis von Kalzium überarbeitet und den Teil des Sensors, der an Kalzium bindet, durch ein Protein ersetzt, das sie kürzlich entdeckt haben und das mehrere Millionen Mal besser an Lanthanide bindet als andere Metalle. Das Protein erfährt eine Formveränderung, wenn es an Lanthanide bindet, was für die Fluoreszenz des Sensors entscheidend ist, um ihn "einzuschalten".
"Der Goldstandard für die Erkennung jedes Elements, das in einer Probe vorhanden ist, ist eine Massenspektrometrietechnik namens ICP-MS", sagt Cotruvo. "Diese Technik ist sehr empfindlich, aber sie erfordert spezielle Instrumente, die die meisten Labore nicht haben, und sie ist nicht billig. Der von uns entwickelte proteinbasierte Sensor ermöglicht es uns, die Gesamtmenge an Lanthaniden in einer Probe zu erfassen. Es identifiziert nicht jedes einzelne Element, aber es kann schnell und kostengünstig am Ort der Probenahme durchgeführt werden."
Mit dem Sensor untersuchte das Forschungsteam auch die Biologie einer Bakterienart, die Lanthanide verwendet - die Bakterien, aus denen das lanthanidbindende Protein ursprünglich entdeckt wurde. Frühere Studien hatten Lanthanide im Periplasma der Bakterien entdeckt - ein Raum zwischen den Membranen in der Nähe der Außenseite der Zelle - aber mit Hilfe des Sensors entdeckte das Team auch Lanthanide im Zytosol der Bakterien - der Flüssigkeit, die die Zelle füllt.
"Wir haben festgestellt, dass die leichtesten der Lanthanide - Lanthan durch Neodym im Periodensystem - in das Zytosol gelangen, die schwereren aber nicht", sagte Cotruvo. "Wir versuchen immer noch zu verstehen, wie und warum das so ist, aber das sagt uns, dass es Proteine im Zytosol gibt, die mit Lanthaniden umgehen, was wir vorher nicht wussten. Das Verständnis dessen, was hinter dieser hohen Aufnahmeselektivität steckt, könnte auch bei der Entwicklung neuer Methoden zur Trennung von Lanthaniden von anderen nützlich sein, was derzeit ein sehr schwieriges Problem ist."
Das Team stellte auch fest, dass die Bakterien Lanthanide aufnehmen, ähnlich wie viele Bakterien Eisen aufnehmen; sie scheiden kleine Moleküle aus, die sich fest an das Metall binden, und der gesamte Komplex wird in die Zelle aufgenommen. Dies zeigt, dass es kleine Moleküle gibt, die wahrscheinlich noch enger an Lanthanide binden als der hochselektive Sensor.
"Wir hoffen, diese kleinen Moleküle und alle Proteine im Zytosol weiter zu untersuchen, die am Ende besser an Lanthanide binden könnten als das Protein, das wir im Sensor verwendet haben", sagt Cotruvo. "Die Untersuchung, wie jedes dieser Produkte mit Lanthaniden bindet und interagiert, kann uns Anregungen geben, wie wir diese Prozesse replizieren können, wenn wir Lanthanide für den Einsatz in aktuellen Technologien sammeln."
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.

























































