Atmende Enzyme im Zeitraffer
Forscher beobachten die Arbeit eines Enzyms in bislang ungesehenem Detail
Wissenschaftler vom Max-Planck-Institut für Struktur und Dynamik der Materie (MPSD) in Hamburg, der Universität Potsdam und der University of Toronto in Kanada haben in einem hochdetaillierten Zeitrafferfilm eines Enzyms sämtliche Teilschritte seines katalytischen Zyklus abgebildet. Ein bemerkenswertes neues Detail: Die Kommunikation zwischen den Proteineinheiten geschieht über eine Kette aus einzelnen Wassermolekülen, vergleichbar mit einem Schnur- oder Dosentelefon. Diese erstaunliche Kommunikation wird von einer ‚Atmungs‘-Bewegung begleitet, also der Ausdehnung und Zusammenziehung des Proteins. Die Zeitraffersequenz der Struktur zeigt, dass dynamische Bewegungen in der Biologie auch auf molekularer Ebene eine zentrale Rolle spielen.
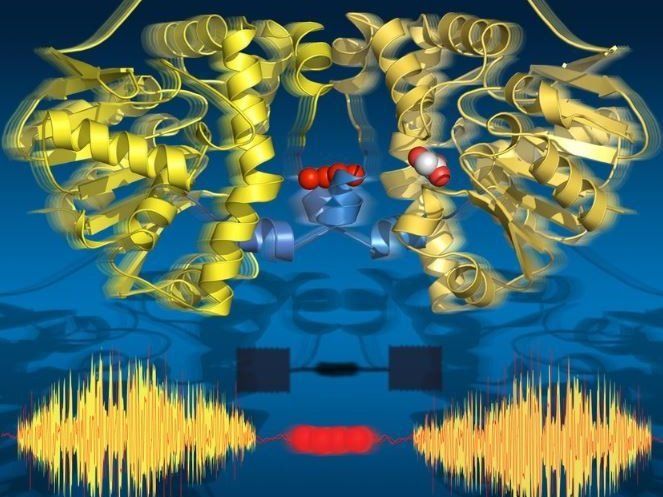
Mit zeitaufgelöster, serieller Synchrotron-Kristallographie können nicht nur alle Schlüsselzustände der enzymatischen Katalyse dargestellt werden - sie zeigt auch, wie die beiden Untereinheiten des Enzyms miteinander kommunizieren.
Das Leben ist dynamisch, genau wie seine molekularen Bausteine. Die Bewegungen und strukturellen Änderungen der Biomoleküle sind ausschlaggebend für ihre Funktionen. Es ist jedoch eine erhebliche Herausforderung, diese dynamischen Bewegungen auf der molekularen Ebene zu verstehen. Wie kann ein Protein eine chemische Reaktion beschleunigen, die ansonsten mehrere Jahre andauern würde?
Mit diesen Themen befasste sich das Team von der Abteilung Atomar Aufgelöster Dynamik des MPSD am Center for Free-Electron Laser Science (CFEL) in Hamburg, der Universität Potsdam und der University of Toronto. Ihre Arbeit ist nun in Science veröffentlicht worden. Sie untersuchten ein Enzym, welches die stärkste Verbindung der organischen Chemie aufspaltet – die C-F-Verbindung der fluorierten Kohlenwasserstoffe.
Diese Verbindungen befinden sich in Materialien wie Teflon oder GoreTex sowie vielen pharmazeutischen Produkten und Pestiziden. Sie sind von besonderer Relevanz für den Klimawandel, wo ihr Einfluss den des CO2 um mehrere Größenordnungen übersteigt.
Sowohl das Verständnis als auch, schlussendlich, die Steuerung der Katalyse der C-F-Verbindungen sind daher von besonderem Interesse für den Klimawandel und die biologische Sanierung.
Mithilfe der zeitaufgelösten Röntgenkristallographie machten die Forscher Schnappschüsse der Katalyse dieses natürlichen Enzyms bei physiologischen Temperaturen. In einem Zeitraum von 30 Millisekunden bis zu 30 Sekunden zeigte dieser Zeitrafferfilm 18 Zeitpunkte, die alle katalytischen Zustände bis zur Aufspaltung der C-F-Verbindung abdeckten.
Zudem beweist der Film überraschenderweise, dass das Enzym während der Katalyse ‚atmet‘, also dass es sich im Takt der katalytischen Teilschritte ausdehnt und wieder zusammenzieht.
Die beiden Hälften des Enzyms kommunizieren zudem über eine Verbindungsschnur von Wassermolekülen. Dieses Wassernetzwerk erlaubt es ihnen, miteinander zu ‚sprechen‘ und Informationen über ihren katalytischen Zustand auszutauschen. Für die Funktion des Enzyms ist dies unerlässlich, da jeweils nur eine seiner Hälften aktiv sein kann.
Diese dynamischen Veränderungen spielen eine wesentliche Rolle in der Funktion des Enzyms. Das Forschungsteam geht davon aus, dass viele andere Systeme ähnliche Mechanismen nutzen.
Originalveröffentlichung
Originalveröffentlichung
P. Mehrabi, E.-C. Schulz, R. Dsouza, H. Müller-Werkmeister, F. Tellkamp, R. J. D. Miller, and E. F. Pai; "Time-resolved crystallography reveals allosteric communication aligned with molecular breathing"; Science; 13. September 2019
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Analytik- und Labortechnik-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.