Leuchtende Bakterienproteine zum Nachweis von Chemikalien im Wasser
Medikamentenreste haben im Wasser nichts zu suchen, Spurenmetalle in Prozesswässern der Recyclingindustrie sind dagegen wertvoll. Wissenschaftler am Helmholtz-Zentrum Dresden-Rossendorf (HZDR) haben ein einfaches Farbsensor-Prinzip entwickelt, mit dem man beide Stoffe sowie viele weitere Substanzen leicht nachweisen kann. Die Idee: Leuchtet die untersuchte Probe rot, ist das Wasser ‚sauber‘; färbt es sich dagegen grün, sind die gesuchten Stoffe enthalten.

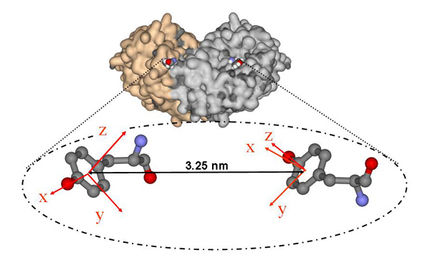
Biosensor: Das am HZDR entwickelte Farbsensor-Prinzip beruht auf einem roten und einem grünen Fluoreszenz-Farbstoff. Wäre ein gesuchter Stoff in einer Wasserprobe vorhanden, würde der Sensor grün leuchten; eine rote Färbung würde dagegen anzeigen, dass die Substanz nicht vorkommt.
HZDR/ Sander Münster 3dkosmos
„Arzneimittelreststoffe werden immer problematischer für die Umwelt. Kläranlagen bauen sie nicht vollständig ab. Das Problem wird zunehmen, betrachtet man z.B. den steigenden Anteil alter Menschen in unserer Gesellschaft und den damit wachsenden Medikamentenverbrauch“, sagt die Leiterin der Arbeitsgruppe Biotechnologie am HZDR, Dr. Katrin Pollmann. „Grundsätzlich eignet sich unser Farbsensor-Prinzip zum Aufspüren aller möglichen Substanzen“, so Pollmann weiter. Gewinnbringend eingesetzt werden könnte es auch beim Recycling strategischer Metalle, einem wichtigen Forschungsthema am Helmholtz-Institut Freiberg für Ressourcentechnologie (HIF) des HZDR, zu dem die Gruppe um Pollmann gehört. In der Recyclingindustrie fallen Prozesswässer an, die Metalle enthalten und die man nutzen kann.
Das Sensorprinzip beruht auf einem roten und einem grünen Fluoreszenz-Farbstoff. Wäre ein gesuchter Stoff in einer Wasserprobe vorhanden, würde der Sensor grün leuchten; eine rote Färbung würde dagegen anzeigen, dass die Substanz nicht vorkommt. Wie kommt es zu dem Farbunterschied? „Die Farbmoleküle befinden sich auf einer nanostrukturierten Oberfläche, die aus bakteriellen Proteinen besteht. Die Farbstoffe liegen so dicht aneinander, dass ein Energieübertrag von den grünen auf die roten Farbstoffe stattfindet, wenn man sie mit Licht einer bestimmten Wellenlänge bestrahlt, z.B. aus einem Laser. Die Probe leuchtet dann rot. Der Energietransfer findet aber nur statt, wenn die Wasserprobe ‚sauber‘ ist. Lagern sich dagegen fremde Substanzen, z.B. die gesuchten Medikamente oder Schadstoffe, zwischen den Farbmolekülen an spezifischen Bindungsstellen an, wird der Transfer unterbrochen und nur die grünen Farbstoffe strahlen“, erklärt Ulrike Weinert. Sie hat sich in ihrer Doktorarbeit mit der Anbindung der Farbmoleküle auf der Nano-Oberfläche beschäftigt.
Das Verbundprojekt („AptaSens“) wurde gefördert durch das Bundesministerium für Bildung und Forschung. Die nanostrukturierte Oberfläche ist ein wichtiger Teil des Projekts. Sie wird aus den Hüllproteinen von Bakterien gewonnen, die die Forscher im Labor heranzüchten. „Die Proteine bilden regelmäßige Gitterstrukturen auf der Nano-Ebene. Sie eignen sich hervorragend, um funktionelle Gruppen und andere Moleküle gleichmäßig anzuordnen“, so Weinert.
Ein wichtiger weiterer Baustein des Sensorprinzips sind die Bindungsstellen auf der Nano-Oberfläche für die nachzuweisenden Substanzen. Dafür werden sogenannte Aptamere eingesetzt. Das sind kurze, einzelsträngige DNA-Oligonukleotide; die DNA-Abschnitte können so gestaltet werden, dass sie in der Lage sind, die unterschiedlichsten Substanzen, wie eben Medikamente oder Schadstoffe, spezifisch zu binden. Sie sind das Spezialgebiet von Dr. Beate Strehlitz vom Helmholtz-Zentrum für Umweltforschung (UFZ) in Leipzig. Im Rahmen des AptaSens-Projektes wurde in ihrer Arbeitsgruppe ein solcher Rezeptor für das Antibiotikum Kanamycin entwickelt, das z.B. zur Behandlung bakterieller Infektionen des Auges, wie Bindehautentzündung, oder in der Tiermedizin eingesetzt wird.
Was nun noch aussteht, ist, den Kanamycin-Rezeptor mit den Farbstoffen zu kombinieren und damit das Farbsensor-Prinzip an einer Beispielsubstanz zu testen. „Ab dann ist es nur noch ein kleiner Schritt bis zur Entwicklung eines vollständigen Farbsensors“, sagt Katrin Pollmann. Dafür müssen die Forscher die einzelnen Komponenten – also Bakterienproteine, Farbstoffe und Aptamer – zu einem Sensorchip integrieren. Sie haben auch bereits mit geeigneten Trägermaterialien, z.B. Glas oder Siliziumdioxid, experimentiert. „Der Sensorchip könnte daumennagelklein sein. Man könnte ihn vor Ort mit einer Wasserprobe, die man untersuchen möchte, benetzen. Dazu gehört dann noch eine Laserlichtquelle, die den Chip aktiviert, und ein Detektor, der die Farbänderung misst“, so Pollmann weiter. Nun bewerben sich die Wissenschaftler um ein Anschlussprojekt.