Femtochemie: Atomballett in Zeitlupe
Mithilfe von kurzen Elektronenpulsen lässt sich eine Strukturänderung in einem komplexen Molekül wie im Film verfolgen
Chemie ist nun filmreif: Mithilfe einer Art Molekülkamera hat ein internationales Team, an dem auch Forscher des Max-Planck-Instituts für Struktur und Dynamik der Materie in Hamburg beteiligt waren, das rasend schnelle Ballett verfolgt, das Atome bei Strukturänderungen in Molekülen vollführen. Mit einer vergleichsweise kompakten, effizienten und kostengünstigen Technik beobachten die Forscher detailliert und in Zeitlupe, wie sich die winzigen Atome bei einem molekularen Übergang in einem komplexen Material bewegen. Solche Umwandlungen der Struktur laufen wie alle chemischen Reaktionen, bei denen Atome ihre Position ändern, in einigen 100 Femtosekunden oder sogar schneller ab. Die Femtochemie kennt zwar heute schon Aufnahmetechniken für chemische Prozesse, dafür sind bislang aber große und teure Anlagen notwendig, in denen nur ausgewählte Projekte erforscht werden können.

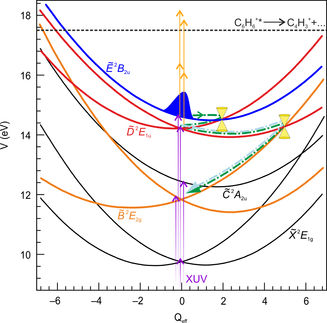
Ein Molekülfilm: Die Einzelbilder zeigen auf’s Atom genau, wie sich Pt(dmit)2-Moleküle innerhalb von einigen 100 Femtosekunden (fs) bewegen, während Me4P[Pt(dmit)2]2 mit Laserlicht vom isolierenden in den metallisch leitenden Zustand umgeschaltet wird. In der Illustration links ist die anfängliche Struktur dargestellt: grau – Platin, schwarz – Kohlenstoff, gelb – Schwefel.
© Science 2015/MPI für Struktur und Dynamik der Materie
„Stellen Sie sich vor, Sie können beobachten, wie Atome sich während eines chemischen Prozesses bewegen!“, schwärmt der Chemieprofessor Dwayne Miller. Genau daran arbeiten der aus Kanada stammende Direktor und seine Mitarbeiter am Max-Planck-Institut für Struktur und Dynamik der Materie seit vielen Jahren. Mit ihrer neuesten Forschungsarbeit, sind die Hamburger Forscher ihrem Ziel einen wichtigen Schritt näher gekommen.
Die Chemie arbeitet heute immer noch weitgehend unbewegten Bildern. Zwar kann sie mit immer feineren Methoden sehr genaue Strukturbilder von Molekülen ermitteln. Doch es sind nur starre Rekonstruktionen der Atompositionen, die den Zustand zum Beispiel vor und nach einem chemischen Prozess zeigen. Mit theoretischen Modellen ließen sich zwar zumindest die Bewegungen kleiner Moleküle während einer chemischen Umwandlung beschreiben. Mit wachsender Zahl der beteiligten Atome explodiert aber auch die Zahl der Freiheitsgrade, mit denen sich die Teilchen in Reaktionen bewegen können. „Diese vielen Freiheitsgrade der Chemie können Physiker in den Wahnsinn treiben“, sagt Miller scherzend, der beide naturwissenschaftliche Denkweisen beherrscht. Eine genaue theoretische Berechnung vieler chemischer Systeme überfordert daher jeden Supercomputer.
So erhellend wie ein Zeitlupenvideo vom Trick eines Magiers
Mit ihrer Technik können die Hamburger Forscher Molekül dagegen filmen und so das schnelle Treiben eines Atomballetts im Detail zeigen. Das ist für die Wissenschaftler so erhellend ist wie ein Zeitlupenvideo, das den Trick eines Magiers offenbart, mit dem er ein Kaninchen aus dem Hut zaubert.
Um die Filmkamera für chemische Prozesse zu entwickeln, mussten Dwayne Miller und seine Mitarbeiter gewaltige experimentelle Herausforderungen meistern: Atombewegungen laufen extrem schnell auf der Zeitskala von einigen Zehn oder sogar Hundert Femtosekunden ab - das ist die Zeit, die Licht braucht, um den Durchmesser eines Haares zu durchqueren.
Die zweite Herausforderung lag in der Winzigkeit der Atome. Dazu muss man mindestens Zehntelnanometer auflösen können – ein Nanometer ist ein Milliardstel Meter. „Würde man einen Apfel bis auf den Durchmesser der Mondumlaufbahn vergrößern, dann wäre eines seiner Atome so groß wie der ursprüngliche Apfel“, veranschaulicht Stuart Hayes das Problem. Der schottische Forscher leitet in Millers Abteilung ein Team, dem gerade das Video eines chemischen Atomballetts gelungen ist.
Die Pump-Probe-Technik war nur wenige Forschungsteams zugänglich
Nun gibt es seit rund dreißig Jahren Aufnahmetechniken für schnelle Atombewegungen, die das Gebiet der Femtochemie begründet haben. Bei der einfachsten Pump-Probe-Technik startet ein erster Pump-Laserblitz den chemischen Prozess, zum Beispiel eine Reaktion. Ihm folgt ein zweiter Probe-Laserblitz, der mit seiner ultrakurzen Femtosekundendauer den aktuellen Zustand wie ein Schnappschuss erfasst. Durch Variieren der Zeitspanne zwischen beiden Blitzen erhalten Forscher die Einzelbilder eines Zeitlupenvideos.
Allerdings hat die Methode mit zwei Laserblitzen einige Nachteile. Die Wellenlänge des Lichts muss sehr kurz sein, damit der zweite Laserblitz einzelne Atome im Bild auflösen kann. Normale Laser erreichen solche Wellenlängen vom extremen Ultravioletten bis in den harten Röntgenbereich hinein nicht. Ein weiteres Problem ist die notwendige Helligkeit des zweiten Lichtblitzes. „Je kürzer die Aufnahmezeit ist, desto hellere Blitze braucht man“, erklärt Miller. Dies zusammengenommen erfordert große, teure Anlagen, sogenannte Freie-Elektronen-Laser. Schon ihre geringe Zahl bietet nur relativ wenigen Forschungsteams einen zeitlich begrenzten Zugang. Aus Sicht der Chemie ist das ein kritischer Flaschenhals, denn die Zaubertricks vieler chemischer Reaktionen warten darauf, aufgedeckt zu werden.
Die Idee: Femtosekunden-Elektronenblitze statt Laserpulse
Dwayne Miller kam deshalb vor Jahren auf die Idee, die Pump-Probe-Methode abzuwandeln. Er ersetzt in seiner Filmkamera für Molekülbewegungen den zweiten Laserblitz durch einen Femtosekunden-Elektronenblitz. Elektronen bieten den Vorteil, dass sie die Lage der Atome in Molekülen direkt abbilden können. Als Quantenteilchen besitzen sie wie Lichtquanten Welleneigenschaften. Doch ihre Wellen sind schon bei geringer Bewegungsenergie so kurz, dass sie problemlos einzelne Atome erfassen und abbilden können. Erzeugen lassen sie sich auf einfache Weise in kompakten Geräten. „Das sind echte Tischexperimente“, sagt Stuart Hayes.
„Trotzdem sind unsere Elektronenkanonen so hell, dass sie die molekulare Struktur in einem einzigen Schuss einfangen können“, ergänzt Miller. Viele Kollegen hätten lange angezweifelt, dass die Methode mit Elektronen funktioniert. Elektronen stoßen sich nämlich wegen ihrer elektrisch gleichen Ladung heftig gegenseitig ab. Dadurch droht eine ursprünglich kompakte Wolke aus einigen tausend Elektronen auf dem Weg zur Probe auseinander zu fliegen. Sie droht die Probe zu lange zu beleuchten, sodass die kurze Blitzzeit, die für eine Femtosekunden-Auflösung nötig ist, nicht erreicht würde. Millers Gruppe löste dieses Problem, indem sie die Flugzeit der Elektronenwolke verkürzte, die Elektronenzahl optimierte und eine Art Optik für Elektronen einsetzte.
Ein Material, das zwischen sich zwischen Isolator und Metall umschalten lässt
Mit dieser Technik haben die Hamburger Wissenschaftler nun ein neues molekulares Material untersucht: Me4P[Pt(dmit)2]2, das kürzlich am japanischen RIKEN-Forschungsinstitut entwickelt wurde. Diese Substanz gehört zu einer interessanten Materialfamilie, deren elektrische Eigenschaften sich zwischen Isolierend, metallisch leitend und in einigen Fällen sogar supraleitend umschalten lassen. Das Umschalten geschieht durch Temperatur oder Druck und wird Phasenübergang genannt. Phasenübergänge kennen wir im Alltag zum Beispiel von Eis, das mit wachsender Temperatur zu Wasser schmilzt. Japanische Wissenschaftler um Tadahiko Ishikawa vom Tokyo Institute of Technology beobachteten kürzlich Folgendes: Me4P[Pt(dmit)2]2 kann unter Laserlicht seine Eigenschaften genauso wechseln wie in einem durch eine Temperaturänderung verursachten Phasenübergang. Dabei wird es von einem elektrischen Isolator zu einem Metall.
Diese Fotoschaltung der Materialeigenschaften können die Forscher nur genau verstehen, wenn sie im Detail verfolgen können, wie sich die einzelnen Atome in den Molekülen verhalten. Genau diese Bewegung haben die Hamburger Wissenschaftler nun erfolgreich abgelichtet. „Wir sehen diese Atome in ihrer Bewegung ganz klar“, sagt Miller, „wie Sterne am Nachthimmel.“ Dabei zeigte sich, dass nur bestimmte Gruppen von Atomen im Kollektiv wenige, koordinierte Schlüsselbewegungen machen, um die Eigenschaften des Materials zu verändern. Genau das ist für Miller die entscheidende Erkenntnis: Die vielen zigtausend Möglichkeiten reduzieren sich auf ein paar einfache, grundlegende Tanzfiguren des atomaren Balletts.
Durch visuelle Beobachtung lassen sich chemische Prozesse besser verstehen
Für Miller bedeutet der Durchbruch zu bewegten Bildern eine konzeptionelle Revolution in der Chemie. Indem die Forscher solche einfachen Bewegungsmuster durch visuelle Beobachtung dingfest machen, können sie chemische Prozesse viel besser verstehen. Der Professor vergleicht das Spielfeld der Möglichkeiten einer chemischen Reaktion mit Tausenden von involvierten Atomen mit einer Berglandschaft. Die Täler repräsentieren verschiedene, stabile Molekülstrukturen. Will sich eine Struktur in der Reaktion verändern, dann muss sie über die Gipfelregionen hinweg in eines der Nachbartäler gelangen. „Dabei reduzieren sich die vielen Möglichkeiten auf einen Passpfad, der am besten zugänglich ist“, erklärt Hayes. Diese Pfade entsprechen den wenigen Grundfiguren des Molekültanzes, den die Videos zeigen.
„Unser jüngster Molekülfilm ist die Krönung jahrelanger Arbeit“, sagt Miller begeistert: „Ich könnte ihn immer wieder ansehen.“ Wer weiß, vielleicht werden solche Aufnahmen in der Geschichte der Chemie eine ähnliche Bedeutung gewinnen die ersten Filme der Gebrüder Lumière für uns, die erstmals unser Leben in Bewegung einfingen.
Originalveröffentlichung
Tadahiko Ishikawa et al.; "Direct Observation of Collective Modes Coupled to Molecular Orbital Driven Charge Transfer"; Science, 18. Dezember 2015