Bisher unbekanntes „Affen-Gen“ im menschlichen Genom entdeckt
Die Entschlüsselung des menschlichen Genoms wurde im Jahr 2001 gefeiert, seitdem sind Genomanalysen viel billiger und besser geworden. Dennoch weiß man wenig darüber, welche DNA-Sequenzen mit bestimmten Krankheiten zusammenhängen. In den Niederlanden wurden jetzt in einer nationalen Studie die Genome von 250 Familien untersucht, dabei kamen einige Milliarden Daten zusammen. Der Saarbrücker Bioinformatiker Tobias Marschall hat gemeinsam mit Forschern aus den Niederlanden diese riesige Datenmenge analysiert, um neue, wiederkehrende und auch fehlende Strukturen zu entdecken. Dabei stießen die Forscher auf ein bisher unbekanntes Gen, das man so bisher nur bei Affen gefunden hat.
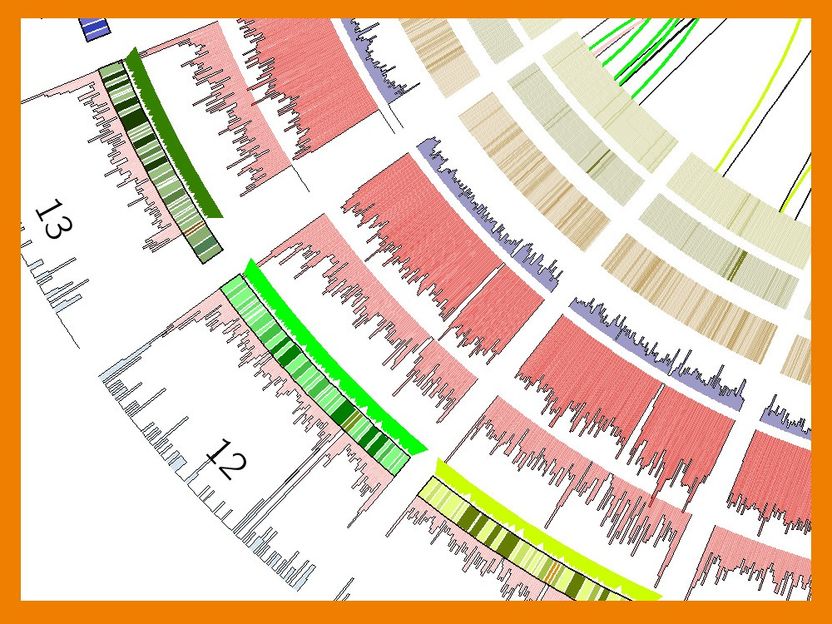
Detail einer Landkarte mit DNA-Varianten
Grafik: Femke Reijnen, ERIBA
„Das menschliche Genom besteht aus etwa drei Milliarden Zeichen. Was viele nicht wissen: Vergleicht man das Erbgut zweier Menschen, so sind ungefähr 99 Prozent dieser Zeichen identisch“, sagt Tobias Marschall, Juniorprofessor am Zentrum für Bioinformatik der Universität des Saarlandes. Diese Varianten im Erbgut können darüber entscheiden, ob man mit einer gewissen Wahrscheinlichkeit eine Krankheit wie etwa Brustkrebs bekommt. Sie können Ärzten aber auch signalisieren, welche Therapie bei einer bestimmten Patientin dann besonders gut ansprechen wird. „Das Interesse an der Gensequenzierung ist daher sehr groß. Durch die von Bioinformatikern entwickelten Rechenverfahren und die immer günstigere Sequenziertechnologie können heute komplette Genomsätze miteinander verglichen werden. Was vor 15 Jahren noch hunderte Millionen Euro pro Datensatz gekostet hätte, ist heute schon für unter tausend Euro zu haben“, erläutert Marschall.
Bei der nationalen Studie in den Niederlanden, die bereits über mehrere Jahre läuft, war die Besonderheit, dass man erstmals in diesem Umfang miteinander verwandte gesunde Menschen verglich. Bei 250 Familien wurde jeweils vom Vater, der Mutter und einem Kind und in einigen Fällen auch von Zwillingskinder das vollständige Genom bestimmt. Denn selbst bei eineiigen Zwillingen ist das Erbmaterial nicht völlig identisch. Gemeinsam mit Forschern des European Institute for the Biology of Ageing (ERIBA) in Groningen sowie weiteren Forschergruppen hat Tobias Marschall diese Rohdaten aufbereitet und nach wiederkehrenden Mustern durchforstet. Um alle Daten extern zu speichern, hätte man rund 7.500 DVDs benötigt. „Man muss sich das so vorstellen, dass ein paar Milliarden Schnipsel wie in einem Puzzle zusammengefügt werden. Während die meisten Genom-Studien bisher nur nach SNPs, kurz ‚Snips‘ genannt, suchten, also nach Unterschieden einzelner Buchstaben im Gencode, ist unser Verfahren viel umfassender“, erklärt Marschall. Die Wissenschaftler suchten im Erbgut der Familien nach größeren zusammenhängenden Strukturen und Besonderheiten, die vor allem in der niederländischen Bevölkerung vorkommen.
„Wir entdeckten dabei nicht nur viele identische Muster, sondern fanden auch Sequenzen, die in einer Generation vorkommen, aber bei der nächsten plötzlich fehlen“, erklärt Marschall. Besonders überraschend war für die Genforscher darüber hinaus ein spezifisches Gen, das man in einer ähnlichen Form bisher nur bei Affen gefunden hatte. „Dieses bisher beim Menschen noch unbekannte DNA-Stück ist offenkundig in der niederländischen Bevölkerung weit verbreitet. Wir konnten es bei rund der Hälfte der 250 untersuchten Familien nachweisen“, sagt der Saarbrücker Bioinformatiker. Die Studie weist nach, dass es im Körper auch für die Produktion von Eiweißen verantwortlich ist. Es ist noch zu erforschen, ob es bei der Entstehung von Krankheiten eine Rolle spielt. Die Forscher vermuten außerdem, dass sich auch die größeren Strukturveränderungen zwischen den kodierenden Abschnitten des Genoms auf bestimmte Krankheiten und ihre Behandlung auswirken könnten.
Weltweit arbeiten derzeit viele Wissenschaftler an so genannten Assoziationsstudien. Dabei wird nach Zusammenhängen zwischen einzelnen DNA-Abschnitten und persönlichen Merkmalen wie dem Risiko für eine bestimmte Krankheit oder der Körpergröße gesucht. „Unsere Forschungsergebnisse werden sich auf diese Studien auswirken, da wir zeigen konnten, wie sich die genannten Strukturveränderungen im Erbgut auf solche Zusammenhänge hin untersuchen lassen“, sagt Marschall.
Die Studie ist Teil des Genom-Projekts der Niederlande (GoNL). Dieses hat zum Ziel, das Erbgut der niederländischen Bevölkerung mit all seinen Variationen zu kartieren. Damit will man die Basis für die personalisierte Medizin der Zukunft schaffen. Mehrere Teams von Bioinformatikern, darunter die Forschergruppe von Tobias Marschall an der Universität des Saarlandes, entwickeln dafür neue Algorithmen. Diese kombinieren sie auf innovative Art und Weise mit bestehenden Rechenverfahren, um die Datenanalyse weiter zu verbessern.