Annäherung an das Geheimnis um gefährliche Blutsyndrome
Genetisch angetriebenes MDS durch Gen, das in Zusammenhang mit dem Zellstoffwechsel steht
Wissenschaftler können auf dem Weg sein, das Geheimnis einer Gruppe von meist unheilbaren Blutkrankheiten, den so genannten myelodysplastischen Syndromen (MDS), zu lösen, die bei den Menschen zu unreifen, gestörten Knochenmarkzellen führen, die eine Vielzahl von Gesundheitsproblemen verursachen und zu Leukämie führen können.
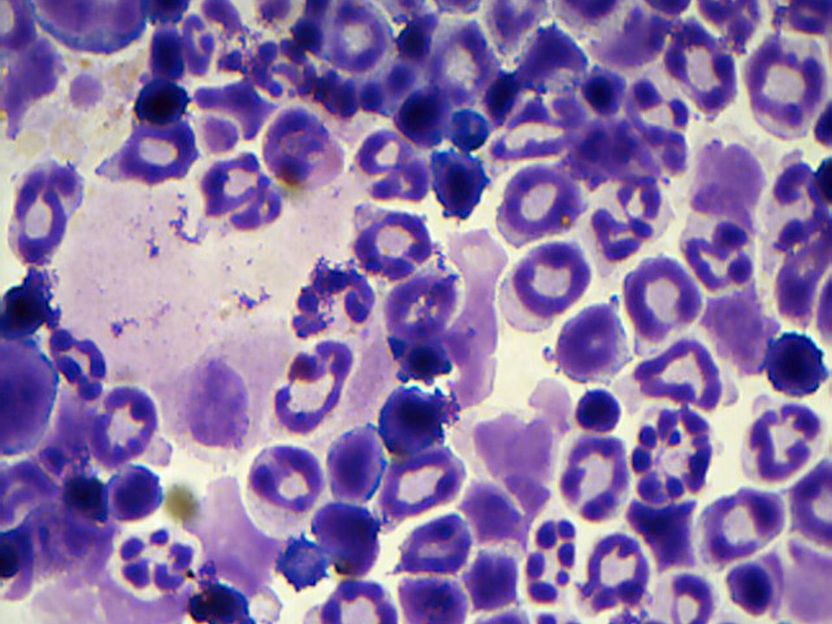
Diese mikroskopische Aufnahme von myeloischen Zellen aus einem genetischen Mausmodell zeigt Anzeichen der Blutkrankheit MDS (myelodysplastische Syndrome), die zu Leukämie führen können. Anstelle des normalen Aussehens der myeloischen Blutkörperchen - eine glatte, runde Donutform mit einem einzigen Kern - sind Zellen mit MDS unterentwickelt, haben mehrere Kerne oder sind hyper-segmentiert. Forscher berichten in der Zeitschrift Cancer Discovery, dass ein Gen namens HIF1A, das molekulare Prozesse antreibt, die zu den verschiedenen Arten von MDS-Erkrankungen führen, die Menschen betreffen, und damit die zukünftige Möglichkeit eröffnet, neue Therapeutika für MDS zu entwickeln.
Cincinnati Children's
MDS ist mit einer Reihe von Genmutationen verbunden und gilt als eine der komplexesten bösartigen Erkrankungen, die blutbildende hämatopoetische Stammzellen im Knochenmark betreffen, so Gang Huang, PhD, ein Krebsbiologe am Cincinnati Children's Hospital Medical Center. Es identifiziert ein Gen, das in Laborexperimenten die biologischen Prozesse antreibt, die die verschiedenen Arten von MDS verursachen, die Ärzte bei Patienten beobachten.
"Wir wissen, dass die Genome von MDS-Patienten wiederkehrende Mutationen in verschiedenen transkriptionellen, epigenetischen und metabolischen Regulatoren aufweisen, aber die Häufigkeit dieser Mutationen entspricht nicht direkt der Krankheit, wenn sie auftritt", sagt Huang, ein Mitglied der Abteilungen Pathologie und Experimentelle Hämatologie und Krebsbiologie. "Unsere Studie zeigt, dass Fehlfunktionen in der Signalgebung von HIF1A die vielfältigen medizinischen Probleme hervorrufen könnten, die Ärzte bei MDS-Patienten sehen."
MDS ist immer häufiger mit zunehmendem Alter der Bevölkerung, mit dem mittleren Alter des Auftretens bei etwa 70 Jahren, so die Forscher. Die einzige Heilmethode ist eine Knochenmarktransplantation, aber sie ist nur in seltenen Fällen sinnvoll, da ältere Patienten mit MDS nicht gesund genug sind, um die Transplantation hämatopoetischer Stammzellen zu tolerieren.
Stoffwechsel- und Sauerstoffregulator
HIF1A (Hypoxie-induzierbarer Faktor 1 alpha) ist ein Transkriptionsfaktor, ein regulatorisches Gen, das anderen Genen sagt, was sie tun sollen. HIF1A spielt eine wichtige Rolle bei der Reaktion der Zellen auf Stoffwechselveränderungen und Sauerstoff und beeinflusst die Funktion von mehr als tausend Genen. Dazu gehört auch eine wichtige Rolle bei der Regulierung biologischer Funktionen in blutbildenden hämatopoetischen Stammzellen im Knochenmark.
Huang und seine Kollegen identifizierten zunächst die zentrale Rolle von HIF1A, indem sie die gespendeten Zellen von MDS-Patienten untersuchten. Dazu gehörte eine umfassende Analyse des Transkriptoms der Zellen (eine vollständige Liste der Boten-RNA-Moleküle, die aus den Genen in einem Organismus exprimiert werden) und des Epigenoms (die Sammlung von Substanzen, die helfen, Gene in Zellen zu regulieren).
Die Wissenschaftler fanden Hinweise auf dysreguliertes HIF1A in den Patientenzellen. Dies führte zu Experimenten in verschiedenen genetischen Mausmodellen, um den Beginn des MDS und seiner genetischen und molekularen Treiber zu untersuchen. Diese Tests bestätigten, dass die Dysregulation von HIF1A eine zentrale Rolle bei der Entstehung spielt, einschließlich verschiedener Manifestationen und Symptome bei Patienten.
Mögliches therapeutisches Ziel
Obwohl die Autoren betonen, dass Jahre zusätzlicher Forschung notwendig sind, bevor sie wissen, ob ihre Ergebnisse klinisch relevant werden, weist ihre Studie auf HIF1A als potenzielles therapeutisches Ziel für eine Krankheit hin, die neue und verbesserte therapeutische Optionen benötigt. Sie ermittelten dies durch die genetische und chemische Eliminierung von HIF1A-Signalen aus ihren genetischen Mausmodellen von MDS. Die Wissenschaftler berichten, dass die Hemmung von HIF1A ein breites Spektrum von MDS-Symptomen umgekehrt hat.
Huang sagte, die nächste Herausforderung für Forscher sei es, ein HIF1A-spezifisches Therapeutikum zur Behandlung von MDS zu identifizieren. Derzeit zielen die meisten kleinmolekularen Inhibitoren von HIF1A sowohl auf sie als auch auf ein zweites verwandtes Molekül namens HIF2A, was sie für MDS-Patienten ungeeignet machen würde.