Medikamente individuell dosieren
Biosensoren könnten in Zukunft eine personalisierte Antibiotikatherapie ermöglichen
Personalisierte Medikamententherapien, bei welchen die Dosis, die Dosierungsintervalle und die Dauer der Behandlung individuell an die Bedürfnisse der angepasst werden, stellen sich zunehmend als vielversprechend dar. Häufig werden Medikamente so dosiert, dass jeder Patient die gleiche standardisierte Wirkstoffmenge erhält. Dabei werden jedoch oft die individuellen Aspekte, beispielsweise der Gesundheitszustand, die Stoffwechselfunktion oder andere körperliche Voraussetzungen der Patienten, nicht ausreichend berücksichtigt. Ein Freiburger Forschungsteam hat nun ein bioanalytisches Verfahren entwickelt, das die Klasse der ß-Laktam-Antibiotika in menschlichem Blut vor Ort – etwa direkt im Operationssaal oder Intensivstation sowie in Arztpraxen oder bei Hausbesuchen – nachweisen kann. „So können wir einfach bestimmen, wie schnell der Körper eines Menschen den Wirkstoff abbaut“, erläutert der Mikrosystemtechniker Dr. Can Dincer, der das Team leitet.
Symbolbild
frolicsomepl, pixabay.com, CC0
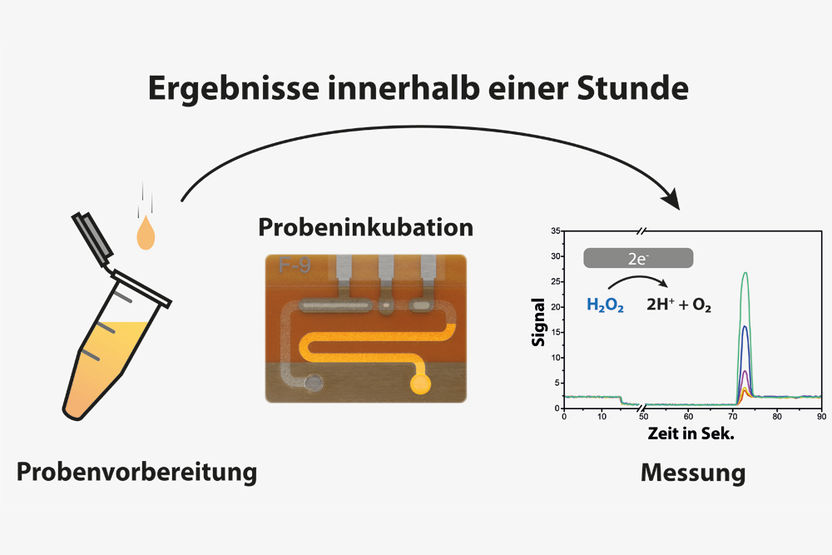
Illustration des Point-of-Care-Testing-Szenarios.
IMTEK – Professur für Sensoren
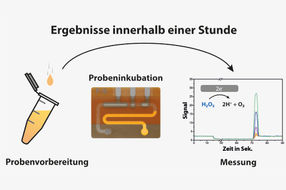
Mit dem neuen Verfahren kann die notwendige Dosis des Medikaments bei einer Therapie individuell auf jeden Patienten abgestimmt werden. „Wir haben die Anwendbarkeit unseres Systems für eine personalisierte Antibiotikatherapie nachgewiesen, indem wir bei zwei Patienten, die während einer Operation mit ß-Lactam-Antibiotika behandelt wurden, den Abbau des Medikaments im Körper vor Ort gemessen haben“, sagt Dincer. „Auf diesen Erkenntnissen aufbauend wollen wir als nächsten Schritt mit einer Kohorten-Studie die Nützlichkeit einer personalisierten Antibiotikatherapie quantitativ bewerten.“
Bereits Ende 2016 hatte das Forschungsteam seine Biosensor-Technologie vorgestellt, die den gleichzeitigen und schnellen Nachweis verschiedener Antibiotika in menschlichem Blut ermöglicht. In der nun veröffentlichten Arbeit haben die Wissenschaftler ihr System mit einem anderen natürlichen Sensor-Protein weiterentwickelt, um ß-Laktam-Antibiotika zu quantifizieren. Die ß-Laktame werden häufig für die Prophylaxe und Behandlung von Infektionskrankheiten in der Humanmedizin eingesetzt.
An dieser fächerübergreifenden Studie waren neun Forschende der Universität Freiburg beteiligt: Richard Bruch, André Kling, Dr. Can Dincer und Prof. Dr. Gerald Urban von der Professur für Sensoren am Institut für Mikrosystemtechnik (IMTEK), Balder Rebmann, Dr. Claire Chatelle und Prof. Dr. Wilfried Weber aus der Abteilung für Synthetische Biologie am Exzellenzcluster BIOSS Centre for Biological Signalling Studies und der Fakultät für Biologie sowie Dr. Steffen Wirth und Prof. Dr. Stefan Schumann aus der Klinik für Anästhesiologie und Intensivmedizin des Universitätsklinikums Freiburg.
Originalveröffentlichung
Meistgelesene News
Originalveröffentlichung
Richard, Bruch, Claire Chatelle, André Kling, Balder Rebmann, Steffen Wirth, Stefan Schumann, Wilfried Weber, Can Dincer, und Gerald Urban; "Clinical on-site monitoring of ß-lactam antibiotics for a personalized antibiotherapy"; Sci. Rep.; 7, 3127; 2017
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

Octet SF3 von Sartorius
Molekulare Bindungskinetik und Affinität mit einer einzigen dynamischen SPR-Injektion
Die Kurvenkrümmung ist der Schlüssel akkurater biomolekularer Wechselwirkungsanalyse

Octet RH16 and RH96 von Sartorius
Effiziente Proteinanalyse im Hochdurchsatz zur Prozessoptimierung und Herstellungskontrolle
Markierungsfreie Protein-Quantifizierung und Charakterisierung von Protein-Protein Wechselwirkungen

Octet R2 / Octet R4 / Octet R8 von Sartorius
Vollgas auf 2, 4 oder 8 Kanälen: Molekulare Wechselwirkungen markierungsfrei in Echtzeit analysieren
Innovative markierungsfreie Echtzeit-Quantifizierung, Bindungskinetik und schnelle Screening-Assays

Holen Sie sich die Analytik- und Labortechnik-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.