Rezeptorsignale in Nervenzellen steuern und sichtbar machen
Neues Werkzeug schlägt zwei Fliegen mit einer Klappe
Mit einem neuen optogenetischen Werkzeug ist es Wissenschaftlern gelungen, die Signale von Serotoninrezeptoren in Nervenzellen zu steuern, nachzuahmen und sichtbar zu machen. Sie modifizierten einen lichtempfindlichen Membranrezeptor aus dem Auge namens Melanopsin. Anschließend konnte dieser durch Licht an- und ausgeschaltet werden und über Fluoreszenz anzeigen, ob bestimmte Signalwege in der Zelle aktiviert worden waren. Der Sensor war des Weiteren so designt, dass er gezielt an die Stellen der Nervenzellen wanderte, die empfänglich für den Botenstoff Serotonin sind. Die Arbeiten beschreibt das Team der Ruhr-Universität Bochum um Dennis Eickelbeck und Prof. Dr. Stefan Herlitze in der Zeitschrift Nature Communications Biology.

Dennis Eickelbeck (links) und Stefan Herlitze bringen Zellen zum Leuchten – mit der sogenannten Optogenetik.
© RUB, Marquard
Signalwege mit Licht aktivieren
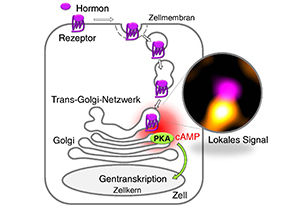
Bei Melanospin handelt es sich um einen G-Protein-gekoppelten Rezeptor, der in Zellen bestimmte Signalwege steuern kann. Bereits in früheren Studien hatte das Bochumer Team vom Lehrstuhl für Allgemeine Zoologie und Neurobiologie den Rezeptor als optogenetisches Werkzeug eingesetzt. Die Biologen hatten den Rezeptor so verändert, dass er sich mit blauem Licht an- und mit gelbem Licht ausschalten ließ. Auf diese Weise konnten sie verschiedene G-Protein-gekoppelte Signalwege in Nervenzellen mit Licht aktivieren.
In der aktuellen Studie entwickelten die Forscher das Werkzeug zu einem Sensor weiter, der anzeigt, ob ein G-Protein-gekoppelter Signalweg angeschaltet wurde. Der Trick: Ist ein solcher Signalweg aktiviert, steigt die Konzentration von Calcium-Ionen in der Zelle. Die Wissenschaftler verschmolzen das Melanopsin mit einem Calcium-Indikator-Protein, welches umso stärker grün fluoresziert, je höher die Calcium-Konzentration in der Zelle ist. Ein grünes Leuchten zeigte somit die Aktivierung eines G-Protein-gekoppelten Signalwegs an.
Doppelter Farbcode
Dann erweiterten die Biologen ihren Sensor – den Calcium-Melanopsin-lokal-Sensor, kurz Camello – noch um zwei weitere Funktionen. Sie bauten ein zweites Fluoreszenzprotein ein, das dauerhaft rot leuchtet. Anhand des roten Leuchtens konnten sie den Sensor in den Zellen lokalisieren, und zwar unabhängig davon, ob ein Signalweg angeschaltet war oder nicht. Ein rotes Leuchten bedeutete somit, dass der Camello-Sensor anwesend war, ein zusätzliches grünes Leuchten, dass er Signalwege aktiviert hatte.
Rezeptor an bestimmte Bereiche transportieren
Zuletzt fügten die Forscher ein Fragment eines Serotoninrezeptors zu Camello hinzu. Das sorgte dafür, dass der Sensor genau in die Bereiche der Zelle transportiert wurde, wo natürlicherweise Serotoninrezeptoren vorkommen. „Serotonin ist im Zentralnervensystem an vielen Prozessen beteiligt und somit auch in die Entstehung vieler Krankheiten involviert, etwa Depressionen, Schizophrenie, Angststörungen oder Migräne. Wir hoffen, dass unser Werkzeug künftig dazu beitragen kann, den Transport, die Lokalisation und die Aktivität beteiligter Rezeptoren genauer zu untersuchen, und es uns dadurch erlaubt wird, die zugrunde liegenden Mechanismen hinter diesen Krankheiten besser zu verstehen“, sagt Dennis Eickelbeck.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Analytik- und Labortechnik-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.