Zelluläre Kommunikationsmittel
Dem NO-Signalweg auf der Spur
Nicht nur Stickstoffmonoxid (NO), auch Schwefelwasserstoff (H2S) agiert als gasförmiges Signalmolekül mit ganz ähnlichen physiologischen Wirkungen. Viele der entscheidenden Fragen über ihr Zusammenspiel hängen von ihrer chemischen Reaktivität und der flüchtigen Existenz von HSNO ab, einem Schlüsselprodukt der Reaktion zwischen beiden. Durch Bindung an einen Zink-Komplex konnte ein Forschungsteam jetzt zwei mit diesem Signalweg in Verbindung stehende Spezies stabilisieren, isolieren und charakterisieren, wie sie in der Zeitschrift Angewandte Chemie berichten.
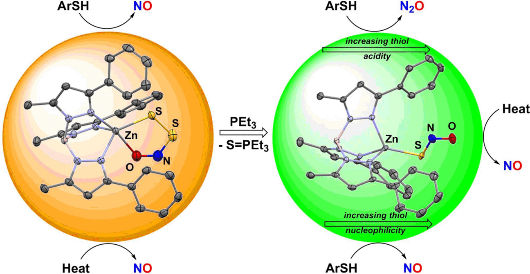
© Wiley-VCH
NO ist ein zentrales Signalmolekül in der Biologie, das eine Vielzahl verschiedener physiologischer Funktionen reguliert, wie Gefäßerweiterung, Weiterleitung von Nervenimpulsen und Zellschutz. Interessanterweise zeigt H2S die gleichen Effekte, es entspannt glatte Muskelzellen, die bei der Gefäßerweiterung eine Rolle spielen. HSNO könnte daher eine der Schlüsselrollen bei der Überschneidung dieser Signalwege spielen. Diese extrem reaktive Spezies ist jedoch so instabil, dass ihre Biochemie und Reaktionswege nur sehr schwer zu entschlüsseln sind. HSNO dringt leicht durch Zellmembranen und kann Proteine nitrosylieren, indem es seine Nitrosylgruppe (-N=O) auf andere Seitengruppen überträgt, vor allem auf Cystein – ein wichtiger Schritt bei verschiedenen zellulären Regulationsmechanismen. Bei physiologischen pH-Werten liegt HSNO vermutlich als Thionitrit-Anion SNO− vor, das instabil ist und leicht in das Perthionitrit-Anion SSNO– umgewandelt wird.
Timothy H. Warren und Valiallah Hosseininasab von der Georgetown University (Washington, DC, USA) stabilisierten die Anionen SNO− und SSNO− durch eine Bindung an einen speziellen Zink-Komplex, der durch eine gängige Umgebung für Zink in der Biologie inspiriert war. Zink ist ein wichtiges physiologisches Metall, das an unzähligen Prozessen beteiligt ist, u.a. an der Regulierung des pH-Werts von Blut. Zudem reagieren Moleküle, die am NO-Signalweg beteiligt sind, wie H2S und S-Nitrosothiole (Moleküle mit einer –S–N=O Gruppe), leicht mit Zink-Schwefel-Bindungen. Diese bilden wichtige strukturelle Einheiten, deren Modifikation in Proteinen zu funktionellen Änderungen führen.
Das Georgetown-Team zeigte, dass Zink-Komplexe, die SNO−- und SSNO−-Anionen enthalten, isoliert und charakterisiert werden können. Die Untersuchung ihrer Reaktivitätsmuster ergab interessante Unterschiede ihrer Reaktionen mit Thiolen (Substanzen mit einer Schwefelwasserstoff-Gruppe –SH), allgegenwärtigen Antioxidanzien, die helfen, Zellschäden zu vermeiden. Währand Reaktionen mit Perthionitrit NO bilden, bildet Thionitrit entweder Distickstoffmonoxid (Lachgas) N2O oder S-Nitrosothiole, die als Reservoir für NO dienen. Diese Ergebnisse lassen vermuten, dass kleinste Unterschiede im Verlauf physiologischer Signalwege zu unterschiedlichen „ausgegebenen Signalen“ führen können, die letztlich aus einem Zusammenspiel von NO und H2S resultieren.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Analytik- und Labortechnik-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
























































