Lastenaufzug hilft Bakterien eine Tarnkappe zu bauen
„Unsere Ergebnisse stellen einen echten Durchbruch dar, da schon seit circa 20 Jahren versucht wurde die Struktur eines TRAP Transporters zu entschlüsseln“
Der Transport von Substanzen über die Membran in die Zelle ist an spezifische Membrantransportproteine gebunden. Forschenden des Universitätsklinikums Bonn (UKB) und der Universität Bonn ist es nun in Zusammenarbeit mit einem internationalen Team gelungen, die molekulare Struktur einer ganz neuen Klasse von solchen Membrantransportern aufzuklären. Beteiligt waren neben den Bonner Wissenschaftler auch Forschende der Universität York. Die Studie ist jetzt im Fachmagazin „Nature Communications“ erschienen.

(v. li) PD Dr. Gregor Hagelueken und Dr. Martin Peter sind im Labor einem bakteriellen Lastenaufzug auf der Spur, der Krankheitserregern hilft, sich vor unserem Immunsystem zu verstecken.
Johann Saba
Wie alle Zellen sind auch Bakterien von einer Zellmembran umgeben. Diese dünne Fettschicht hält Nährstoffe, Erbmaterial und Eiweiße der Zelle zusammen und ermöglicht so erst ihr Überleben. Andererseits müssen zum Beispiel Nährstoffe oder Moleküle, die als Bausteine für die Zelle dienen, die Membran überqueren können, sonst würde die Bakterie buchstäblich verhungern. Zu diesem Zweck bedienen sich Zellen sogenannter Membrantransporter. Das sind Eiweißmoleküle, welche in der Zellmembran sitzen und mit komplizierten Bewegungen Stoffe über die Membranbarriere transportieren. Die sogenannten TRAP Transporter helfen Krankheitserregern wie Haemophilus influenzae oder Vibrio cholerae ein kleines Zuckermolekül namens Sialinsäure über die Zellmembran zu bewegen. Sialinsäure kommt in menschlichem Gewebe sehr häufig vor und die Bakterien können sie mit dem TRAP Transporter förmlich aufsammeln und in ihre Zellwand einbauen. „Dort dient sie der Bakterie als eine Art Tarnkappe, um sich vor unserem Immunsystem verstecken zu können“, sagt der Bonner Wissenschaftler PD Dr Gregor Hagelueken.
Bakterieller Lastenaufzug live bei der Arbeit
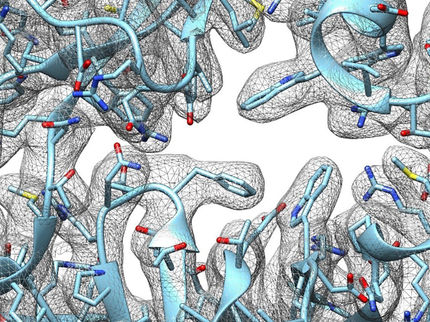
Die Forschenden aus der Arbeitsgruppe von Hagelueken am Institut für Strukturbiologie des UKB benutzten die sogenannte cryo-Elektronenmikroskopie um die Struktur des Transporters zu entschlüsseln. „Unsere Ergebnisse stellen einen echten Durchbruch dar, da schon seit circa 20 Jahren versucht wurde die Struktur eines TRAP Transporters zu entschlüsseln“, sagt der Bonner Post-Doktorand Martin Peter. Er erinnert sich an den Moment als klar war, dass die Mammutaufgabe bewältigt war: „In diesem Augenblick waren wir die ersten, die jemals einen TRAP Transporter gesehen haben. Uns war dann sofort klar, wie das Eiweiß funktioniert. Es bewegt sich wie ein Aufzug in der Membran auf und ab.“
In Zusammenarbeit mit der Arbeitsgruppe von Prof. Dr. Ulrich Kubitscheck am Clausius Institut für Physikalische und Theoretische Chemie der Universität Bonn konnten die Forschenden dem Transporter live bei der Arbeit zusehen. „Der TRAP Transporter kommt in vielen krankmachenden Bakterien vor“, sagt Hagelueken, „vielleicht kann unsere Struktur in Zukunft dabei helfen, Antibiotika zu entwickeln, die dafür sorgen, dass der Aufzug stecken bleibt.“
Originalveröffentlichung
Martin F. Peter, Jan A. Ruland, Peer Depping, Niels Schneberger, Emmanuele Severi, Jonas Moecking, Karl Gatterdam, Sarah Tindall, Alexandre Durand, Veronika Heinz, Jan Peter Siebrasse, Paul-Albert Koenig, Matthias Geyer, Christine Ziegler, Ulrich Kubitscheck, Gavin H. Thomas & Gregor Hagelueken: Structural and mechanistic analysis of a tripartite ATP-independent periplasmic TRAP transporter; Nature Communications; 2022
Originalveröffentlichung
Martin F. Peter, Jan A. Ruland, Peer Depping, Niels Schneberger, Emmanuele Severi, Jonas Moecking, Karl Gatterdam, Sarah Tindall, Alexandre Durand, Veronika Heinz, Jan Peter Siebrasse, Paul-Albert Koenig, Matthias Geyer, Christine Ziegler, Ulrich Kubitscheck, Gavin H. Thomas & Gregor Hagelueken: Structural and mechanistic analysis of a tripartite ATP-independent periplasmic TRAP transporter; Nature Communications; 2022
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Analytik- und Labortechnik-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.



















![[Fe]-Hydrogenase-Katalyse mittels Parawasserstoff-verstärkter Kernmagnetresonanzspektroskopie sichtbar gemacht](https://img.chemie.de/Portal/News/675fd46b9b54f_sBuG8s4sS.png?tr=w-712,h-534,cm-extract,x-0,y-16:n-xl)
































